锂氧电池是如何工作的?一文揭晓其中的猫腻
随着锂离子电池能量密度的提高,传统的"含锂氧化物/石墨"电池结构已经难以满足高比能量锂离子电池的需求。在众多的新型高比能量电池中,Li-O2电池是其中佼佼者,比能量可以达到900Wh/kg以上,远超现有的锂离子电池技术。
Li-O2电池之所以有如此该的比能量主要是得益于其正极材料O2在空气中的储量几乎是"无限"的,因此正极的比容量也就是"无限"的,所以Li-O2电池容量的唯一的限制因素就是负极Li的数量。Li-O2电池的性能受到很多因素的影响,包括正极的反应机理、反应产物的形貌等因素都会对锂空气电池的放电特性产生较大的影响,而这些因素都主要依赖于电解液的选择。
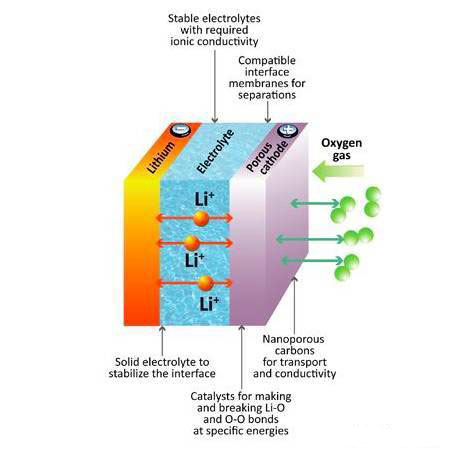
来自美国西北太平洋国家实验室的Langli Luo等人近日利用环境透射电子显微镜对全固态Li-O2电池的反应机理进行了研究,研究显示在CNT表面首先形成LiO2化合物,随后该产物发生歧化反应生成Li2O2和O2,O2的释放生成了一个外层由Li2O构成,内层由Li2O2构成的中空球状结构。目前该型研究成果已经发表在了最新的Natural Nanotechnology杂志上。

环境透射电子显微镜能够在氧气环境下进行工作,从而使得在原子级别对锂氧电池的反应过程进行直接的观测成为可能。实验中Langli Luo利用载有纳米RuO2催化剂的CNT作为正极,金属Li作为负极,金属Li表层的Li2O作为固体电解质,电池结构如下图所示。
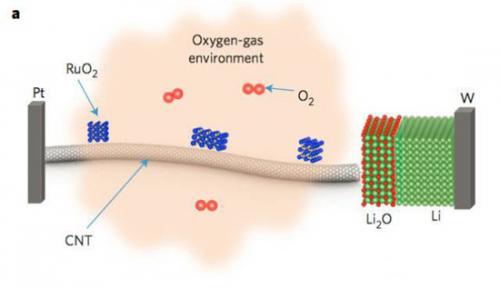
反应产物的形成过程如下图所示,从图上我们可以注意到,在反应开始不久后,就在三相界面出现了一个中空的球,随后这个球持续长大,从一开始直径50nm到最后生长到了200nm,随后该中空球结构开始收缩和坍塌。目前还不清楚,为何反应产物不形成固体颗粒或者是层状结构。为了对这其中的机理进行深入的理解,Langli Luo采用了局部电子衍射技术(SAED)对充放电过程中材料的相变进行了研究。
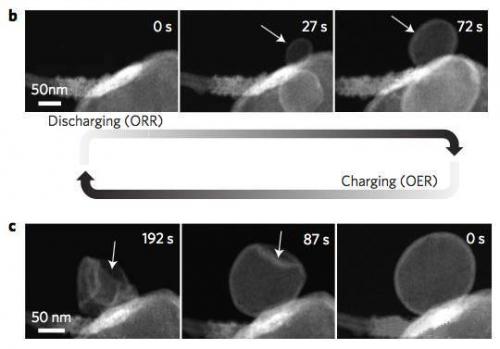
研究显示,初始反应产物LiO2很快会发生歧化反应生成Li2O2和O2,在颗粒内部释放的O2被封锁在了颗粒的内部,从而导致了颗粒成为中空结构,如下图所示。从SAED的分析结果来看,在开始的几秒钟时间内,反应产物中只有LiO2,30秒之后,Li2O2和LiO2开始共存,大约100s后LiO2的衍射峰消失,反应产物只剩下Li2O2和Li2O,TEM分析结果显示中空球的外侧为Li2O,内侧为Li2O2。充电过程则正好相反,开始的时候观察到了Li2O和Li2O2的衍射峰,在48s时出现了LiO2的衍射峰,但是在120s时并没有再出现LiO2的衍射峰,说明LiO2只是Li2O2分解的一个中间产物。整个过程为我们揭示了Li-O2电池的充放电反应途径,在放电的时候,Li+通过电解液扩散到CNT表面,在三相界面发生反应,生成LiO2,然后LiO2发生歧化反应(LiO2?Li2O2+O2),生成Li2O2和O2,反应释放的O2会将反应产物从最初的10nm左右,吹到100nm左右,而在产物的表面由于有丰富的Li+,因此会与O2反应生成Li2O。在充电的过程中,Li2O2首先会失去一个Li+和一个电子,形成LiO2,随后LiO2发生分解,产生Li2O2和O2,然后Li2O2再次失去Li+和电子,如此循环指导所有的Li2O2消耗完毕。
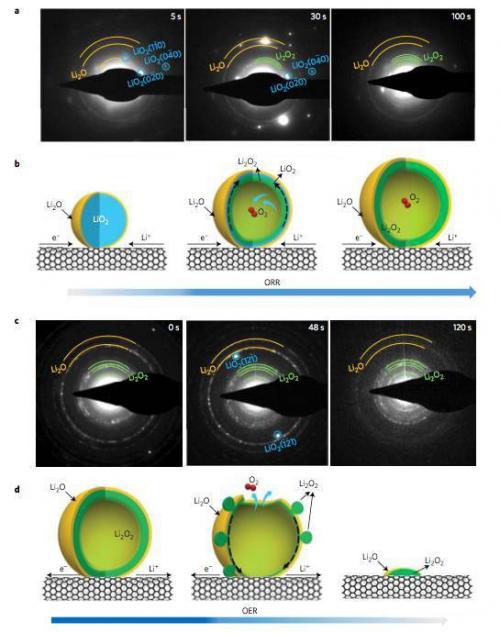
Langli Luo的工作为我们理解Li-O2电池的反应过程和机理作出重要的贡献,对Li-O2电池的电极设计具有重要的参考意义。
- 基于MAX1501的锂离子电池充电器的研制(01-06)
- SBS管理器确保锂离子电池安全高效(02-23)
- 电池基本知识 锂离子电池基础知识大汇萃(09-09)
- 锂离子电池充电器扩流电路设计(02-24)
- 如何选择锂离子充电管理IC(04-29)
- 智能充电管理可以克服便携式设备面临的挑战(05-11)
