 由图2可以看出,在放电电流密度为1.8 mA/cm2时,电解质3的放电容量和电压平台比其它两种电解质的要高。可见,使用低粘度的电解质3放电过程中溶解的多硫化离子能较快地扩散,不会造成多硫化离子在正极区的累积,在电池充放电过程中产生的极化度小。在放电电流密度为1.8 mA/cm2时首放比容量为844 mAh/g,说明电解质3具有很好的大电流性能。
由图2可以看出,在放电电流密度为1.8 mA/cm2时,电解质3的放电容量和电压平台比其它两种电解质的要高。可见,使用低粘度的电解质3放电过程中溶解的多硫化离子能较快地扩散,不会造成多硫化离子在正极区的累积,在电池充放电过程中产生的极化度小。在放电电流密度为1.8 mA/cm2时首放比容量为844 mAh/g,说明电解质3具有很好的大电流性能。

2.2.2 电池的循环性能
图3为三种电解质组装的锂-硫电池存放电电流密度为1.8 mA/cm2时的循环性能曲线。由图3可知,与首次放电比容量相比,第二次放电比容量显著降低,随后的多次循环容量衰减比较缓慢,曲线趋于平缓。容量衰减源于硫硫键断裂产生的多硫离子与负极锂反应,形成了Li2S钝化层覆盖在电极表面,消耗了部分硫。Li2S钝化层是Li+的良好导体,它的形成不会影响反应的正常进行,但是在充电过程中,这部分损失的硫不能被氧化再形成硫硫键;同时隔膜阻塞、自放电、活性物质发生团聚及在电解质中过饱和沉积等现象也会造成循环性能下降。图中电解质1所组装的电池和电解质3所组装的电池第二次放电比容量比第一次放电比容量高,特别是在大电流密度放电时更容易产生。比较合理的解释有两种:一是由于放电电流密度较大,放电时间短,在短时间里电解质还未充分浸润到正极的内层,从而导致第一次放电容量低于第二次放电;另一种解释为,第一次放电时,由于大电流密度放电时间短,放电电流大,正极表面很快形成一层多硫化物的堆积层,锂离子来不及扩散到正极内层与硫反应,导致活性物质硫的利用率低。而在第二次及以后的放电过程中,由于电解质的充分浸润以及电池更趋于稳定状态,则不再出现后一次放电容量比第一次放电容量高的现象,当然前提条件是电池必须正常放电。从图3可以看出,电解质3所组装的电池,在大电流密度下循环性能最好,20次循环后比容量为709 mAh/g,这可能因为该电解质的粘度较低,而且没有电解质2中充电过程中硫溶解性的问题。电解质1所组装的电池,20次循环后比容量在650 mAh/g,也展现了这种电解质良好的循环性能,在大电流循环性能方面也比电解质2好。

2.2.3 电池的充放电效率
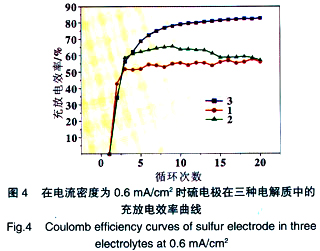
图4为三种电解质在电流密度为0.6 mA/cm2下的放电的充放电效率曲线,由图4可知,电池的充放电效率都是随着循环次数的增加而增大,最后趋于平稳的。前几次的充放电效率都比较低,这是由于前几次电池还没有达到稳定状态,而一部分硫放电后生成不可逆放电产物Li2S,Li2S在电极表面形成不稳定钝化膜,导致过充现象严重,所以效率很低。当放电电流密度为0.6 mA/cm2时,电解质3的充放电效率超过了80%,而电解质1和电解质2明显要低一些。而就电解质1和电解质2来说,电解质2要比电解质1好。
2.2.4 循环伏安测试
由图5可以看出,在这三种电解质中,还原峰在2.4 V和2.0 V两处分别对应了放电曲线中的两个放电电压平台,在2.4~2.5 V之间出现两个氧化峰,也分别对应充电过程中出现的两个充电电压平台。2.0 V的还原峰电位逐渐正移,峰形逐渐变得尖锐,这说明硫在高电导率电解质中的电极极化较小,而电导率只是影响电极极化的一个因素,还可能与电极的表面状态的变化等因素有关。

2.2.5 电池的交流阻抗测试
由图6可以看出,采用电解质2和电解质1组装的电池阻值随放置时间的增长而增大,电解质2要比电解质1的增长幅度大。而电解质3的阻值随放置时间的增长基本上没有太大的变化,电解质3的阻值一直保持在50~80 Ω之间,说明其内阻较小,充放电时产生的极化小,这是因为电解质3有着良好性能。电解质2放置一天后,其阻值达到了280 Ω,说明这种电解质组装的电池其内阻一直在增大,而且幅度相对较大。电解质1的溶液电阻也随放置时间增长而增大,但是增长幅度很小。


3 结论
硫电极在不同电解质中的电化学性能测试结果表明,溶剂组分对硫电极的电化学性能具有一定的影响。硫电极低电压平台的电位和电解质的粘度密切相关。当电解质为1 mol/LLiClO4/(DME+THF)(50:50,体积比)时,硫电极有很好的大电流性能,首放容量高达860 mAh/g,当放电电流密度为0.6mA/cm2时,电解质3的充放电效率超过了80%。
|
|
|
|